La cara oculta de los riesgos de la "vacuna" covid: La respuesta inmune materna conduce a un accidente cerebrovascular neonatal
El Factor Plaquetario 4 (PF4) su papel en la coagulación. Receptores FcγIIa y formación de trombos. Epítopos inmunodominantes y reactividad cruzada.
Desde el amplio ámbito de la medicina contemporánea, donde el dogma de la vacunación ha sido proclamado como uno de los mayores triunfos de la salud pública, surgen casos clínicos que desafían creencias y obligan a todo médico especialista a repensar la relación entre la inmunidad adquirida y los efectos adversos imprevistos. Este artículo aborda un fenómeno poco explorado pero de inmensa relevancia.: la Trombocitopenia Trombótica Inmunitaria Inducida por Vacuna (VITT) en neonatos, una condición que surge cuando anticuerpos maternos anti-PF4, generados tras la vacunación contra la COVID-19, atraviesan la placenta y desencadenan trombosis en el recién nacido.
El objetivo de esta investigación es profundizar en los mecanismos fisiopatológicos, los factores predisponentes y los retos diagnósticos y terapéuticos de esta grave complicación. A través de una revisión exhaustiva de la evidencia científica y un enfoque crítico de la medicina basada en la inmunomodulación, se aborda cómo la producción de anticuerpos patógenos, un proceso diseñado teóricamente para proteger, puede convertirse en uno de los múltiples factores desencadenantes de la enfermedad. Ante este tema, haremos una aproximación desde la interacción molecular entre el Factor Plaquetario 4 (PF4) y los anticuerpos maternos, hasta las implicaciones clínicas, biomarcadores predictivos, estrategias de diagnóstico avanzado y manejo neonatal, con el fin de brindar una guía experta que pueda ser de utilidad para las madres y padres interesados, así como para los médicos que se enfrentan a estos complejos escenarios.
Sabemos que anteriormente un estudio encontró trazas de ARNm de “vacunas” covid en leche materna; publicado en JAMA Pediatrics el 26 de septiembre de 2022. El "Detection of Messenger RNA COVID-19 Vaccines in Human Breast Milk" cuyos autores principales son Nazeeh Hanna y colaboradores, en este trabajo detectaron pequeñas cantidades de ARNm en 7 de 131 muestras analizadas, recolectadas de 11 mujeres antes y después de la vacunación.
Otro estudio “mRNA Vaccines and Breastfeeding: A Prospective Cohort Study" (NPJ Vaccines, agosto de 2021, encontró una transferencia mínima de ARNm de las vacunas a la leche materna, detectándose en menos del 10% de las muestras analizadas.
Otro estudio en el mismo sentido “Detection of SARS-CoV-2 Antibodies and mRNA in Human Milk Following COVID-19 Vaccination" (Frontiers in Immunology, enero de 2022. En este estudio se detectaron niveles bajos y temporales de ARNm en leche materna tras la vacunación En todos los casos se realizaron controles para confirmar que el ARNm detectado correspondía específicamente a las vacunas y no a otras fuentes. Esto incluye el uso de secuenciación o análisis comparativos y en otros casos detectaron el ARNm con reacción en cadena de la polimerasa con transcripción inversa. Aunque los estudios coinciden en que las cantidades son insuficientes para causar daño y respaldan la seguridad de la lactancia tras vacunarse. Sin emabrgo ahora nos encontramos a un bebé con trombocitopenia trombótica inducida por la vacuna que se la aplicó a la madre.
Súmate a este análisis riguroso y reflexivo, donde convergen la ciencia y la ética médica para arrojar luz sobre una realidad que exige ser entendida y abordada con la mayor precisión.
Hoy estamos ante un caso que nos obliga a cuestionar, investigar y analizar con rigor: la trombocitopenia neonatal inducida por anticuerpos anti-PF4 maternos en el contexto de la “vacuna” covid.
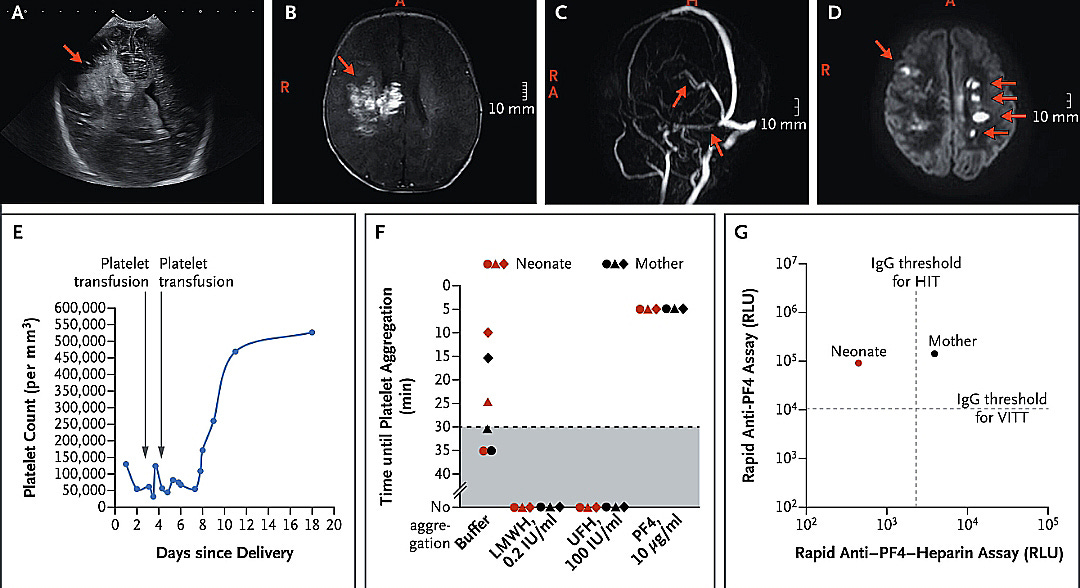
La publicación el 12 de febrero de 2025 en el New England Journal of Medicine del artículo “Anticuerpos anti-PF4 maternos como causa de accidente cerebrovascular neonatal” sobre un neonato afectado por trombosis de senos venosos cerebrales (TSVC) debido a anticuerpos anti-PF4 maternos que atraviesan la placenta es más que un estudio clínico; es un llamado a la reflexión sobre los mecanismos inmunológicos y su impacto en la práctica médica contemporánea.
Anticuerpos anti-PF4 maternos como causa de accidente cerebrovascular neonatal
1. Madre de 35 años con historial de embolia pulmonar y recuento bajo-normal de plaquetas.
2. Neonata nacida por cesárea a las 39 semanas y 2 días con restricción del crecimiento.
3. Presentó hemorragia cerebral y accidentes cerebrovasculares arteriales.
4. Desarrolló trombocitopenia severa y alta actividad de dímero D.
5. No se inició anticoagulación debido a riesgo de hemorragia cerebral.
1. La Biología Oculta: La Relación Entre el PF4 y la Respuesta Inmune
El factor plaquetario 4 (PF4) es una proteína clave en la regulación de la coagulación sanguínea, liberada por los gránulos alfa de las plaquetas. Su papel en la medicina; hematólogos, inmunohematólogos, cardiólogos, especialistas en hemostasia y trombosis, médicos de laboratorio clínico, ginecólgos y especialistas en medicina comunitaria, se ha vuelto más evidente con el hallazgo de que, bajo ciertas condiciones, puede generar inmunocomplejos que activan respuestas autoinmunes.
PF4 y su papel en la coagulación
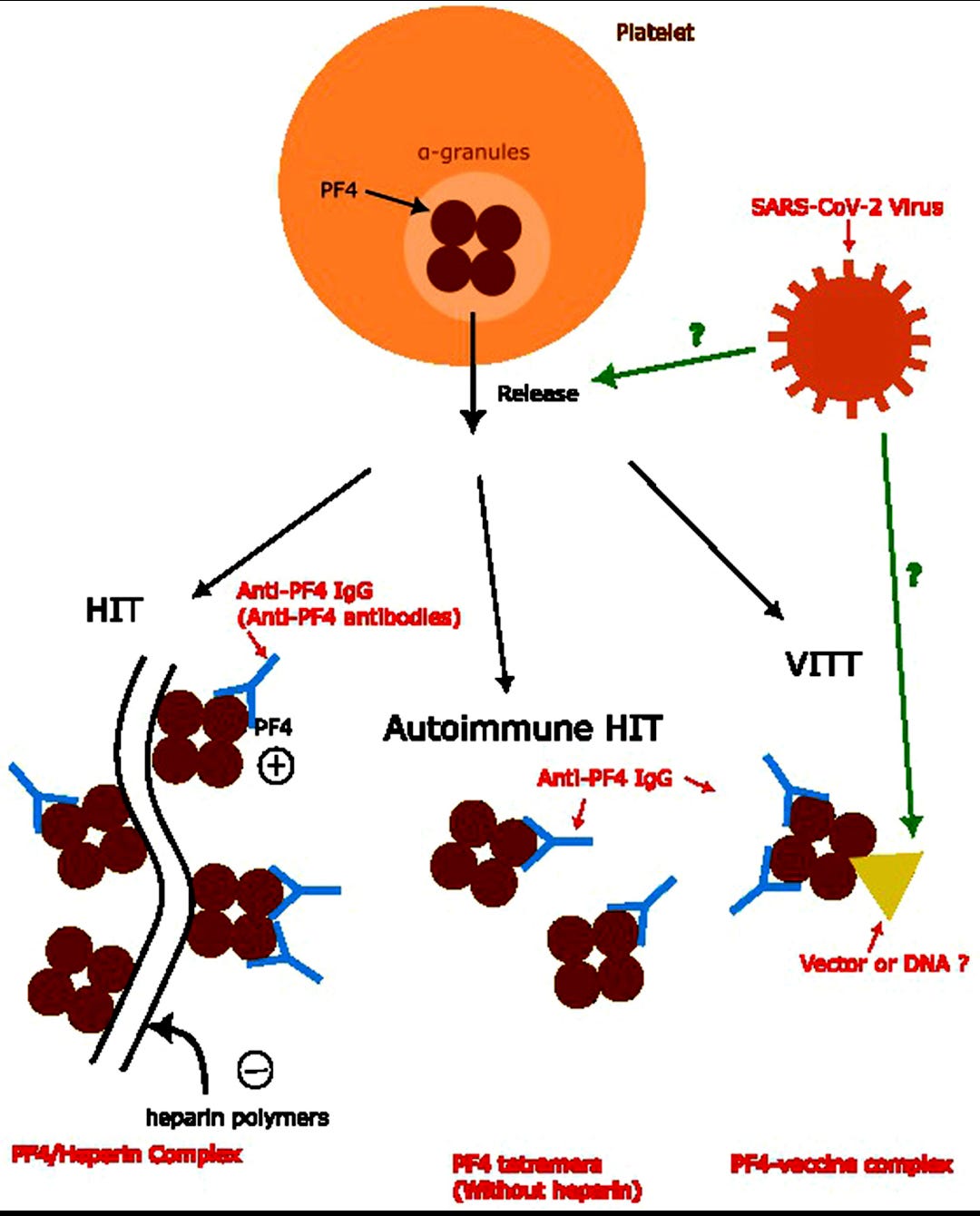
El PF4 o CXCL4 es una proteína de gran importancia en la hemostasia y la regulación de la coagulación sanguínea. Es una pequeña citocina perteneciente a la familia de las quimiocinas CXC caracterizada por tener dos cisteínas (C) separadas por un aminoácido (X) en su extremo N-terminal; L: Indica que es un ligando, interactuando con receptores específicos en las células.; 4: Fue la cuarta quimiocina CXC identificada y caracterizada. Por lo tanto, es el número asignado a esta quimiocina específica dentro. PF4 es una proteína con carga positiva que se une a moléculas cargadas negativamente como el heparán sulfato en el endotelio o la heparina exógena. Esta interacción puede formar complejos que inducen una respuesta inmune anómala, llevando a la producción de anticuerpos anti-PF4. Estos anticuerpos pueden activar plaquetas a través del receptor FcγIIa, promoviendo la agregación plaquetaria y la formación de trombos. El receptor FcγIIa es un tipo específico de receptores Fc; proteínas especializadas que se encuentran en la superficie de diversas células del sistema inmunitario.
El receptor FcγIIa desempeña un papel crucial en la formación de trombos, especialmente en el contexto de la trombocitopenia inducida por vacuna COVID-19 (VITT), cuando los anticuerpos anti-factor plaquetario 4 (anti-PF4) generados tras la vacunación se unen al receptor FcγIIa en la superficie de las plaquetas; esta unión desencadena una potente señal activadora en las plaquetas, iniciando el proceso de inmunotrombosis.
La activación plaquetaria vía FcγIIa provoca la liberación de micro partículas protrombóticas.
Estas micro partículas aumentan la producción de trombina, favoreciendo la formación de trombos
La activación plaquetaria también amplifica la respuesta que causa la liberación de más proteína PF4 de los gránulos plaquetarios, lo que perpetúa el ciclo de formación de complejos PF4-anticuerpo y activación plaquetaria.
El mecanismo de la trombocitopenia trombótica inducida por vacuna VITT es similar al de trombocitopenia trombótica inducida por heparina, donde los anticuerpos anti-PF4 activan las plaquetas a través del receptor FcγIIa. Este proceso se ha demostrado en pacientes con trombosis de venas cerebrales y sinusales después de la “vacuna” covid.
En el contexto de la la trombocitopenia trombótica inducida por vacuna VITT, el receptor FcγIIa actúa como un mediador clave en la cascada de eventos que conducen a la formación de trombos, conectando la respuesta inmune inducida por la vacuna con la activación plaquetaria y la coagulación.
Interacción con otras células
Los complejos antígeno-anticuerpo que interactúan con FcγIIa también pueden activar monocitos.
Esta activación lleva a la producción de factor tisular y daño endotelial, contribuyendo aún más al estado protrombótico
El PF4 puede presentarse como monómero, dímero o tetrámero, dependiendo de su concentración.
La génesis de los anticuerpos anti-PF4
En algunas circunstancias, como la exposición a la heparina o ciertas respuestas inmunitarias atípicas, se generan anticuerpos IgG contra los complejos PF4-heparina o PF4-heparán sulfato. La activación plaquetaria resultante puede desencadenar una trombocitopenia trombótica, una afección que anteriormente se asociaba con la trombocitopenia inducida por heparina (HIT) y, más recientemente, con la trombocitopenia trombótica inmunitaria inducida por vacunas (VITT).
La vacunación y la respuesta autoinmune inesperada
En la intersección de la inmunología y la coagulación, surgen preguntas sobre los efectos secundarios potenciales, particularmente en la esfera de la trombosis inmunomediada.
Hipersensibilidad inmunológica y producción de anticuerpos patológicos
La vacunación en ciertos individuos, puede producir una respuesta que puede volverse patológica y generar autoanticuerpos, lo que da lugar a fenómenos como la trombocitopenia trombótica inmunitaria inducida por vacuna (VITT) y la neuropatía autoinmune post vacunación.
1. La producción de la proteína Spike y su interacción con la coagulación
Las vacunas de ARNm inducen la producción de la proteína Spike en células humanas. No obstante, se ha observado que la proteína Spike puede interactuar con fragmentos celulares derivados de megacariocitos; células grandes y especializadas de la médula ósea cuya función principal es producir plaquetas, y receptores de membrana plaquetaria como las integrinas (especialmente αIIbβ3; conocidas como glicoproteína IIb/IIIa (GPIIb/IIIa), que son receptores cruciales en la superficie de las plaquetas fundamentales para la agregación plaquetaria.
Los megacariocitos extienden prolongaciones llamadas proplaquetas hacia el interior de los vasos sanguíneos sinusoides de la médula ósea.
Estas proplaquetas se fragmentan en el torrente sanguíneo, liberando plaquetas maduras.
En situaciones que requieren un aumento rápido de plaquetas, los megacariocitos pueden experimentar una "fragmentación explosiva", liberando plaquetas preformadas directamente de su citoplasma
Receptores de membrana plaquetaria, especialmente las integrinas αIIbβ3
Mecanismo de acción: Durante la agregación plaquetaria, las integrinas αIIbβ3 de diferentes plaquetas se unen entre sí a través del fibrinógeno, que actúa como puente.
La proteína Spike contiene epítopos inmunodominantes . Un epítopo es una región específica de la proteína que es reconocida por el sistema inmunológico, particularmente por anticuerpos o células T, y puede desencadenar la producción de anticuerpos que reaccionan con estructuras endógenas del cuerpo humano. Es decir la proteína Spike puede contener epítopos que son estructuralmente similares a partes de proteínas humanas. Esto se conoce como "mimetismo molecular" o reactividad cruzada y puede tener implicaciones importantes: Esta similitud puede tener implicaciones importantes:
Puede confundir al sistema inmune, y conllevar potencialmente a reacciones autoinmunes, además de que la vacuna ni te proteja, ni te nmunice de nada.
Interacción entre la proteína Spike y las plaquetas
Es importante comprender la interacción entre la proteína Spike que puede interactuar directamente con las plaquetas, así como sus implicaciones en la coagulación y la respuesta inmune:
Puede promover la activación plaquetaria, especialmente en presencia de otros factores procoagulantes.
Contribuye a un estado de hiperreactividad plaquetaria, lo que puede favorecer la formación de trombos.
Induce un fenotipo inflamatorio en las plaquetas, contribuyendo a un microambiente procoagulante.
La exposición a la proteína Spike a través de la vacunación puede activar fuertemente el sistema inmune innato:
Una activación excesiva puede conducir a una inflamación crónica y desregulación inmunitaria.
En casos graves, se ha observado una hiperinflamación similar al síndrome de liberación de citocinas.
Predisposición genética y autoinmunidad
En individuos con predisposición genética, la vacuna covid podría actuar como un desencadenante de enfermedades autoinmunes latentes:
La vacunación podría provocar una respuesta inflamatoria inmunomediada.
El mimetismo molecular entre la proteína Spike y proteínas endógenas puede ser un mecanismo subyacente.
Neuroinflamación y trastornos neurológicos autoinmunes
En algunos pacientes post vacunación, se han reportado cuadros neurológicos asociados a inflamación inducida por la activación del sistema inmune innato.
Se han reportado casos de manifestaciones neurológicas autoinmunes post-vacunación, Entre ellos:
Síndrome de Guillain-Barré (SGB): Se ha relacionado con vacunas de adenovirus, caracterizado por una respuesta autoinmune contra la mielina periférica.
Miocarditis post-vacunal: Mediado por una respuesta inflamatoria exagerada en el tejido cardíaco, más frecuente en hombres jóvenes tras vacunas de ARNm.
Encefalopatía autoinmune y síndrome postural ortostático taquicárdico (POTS): Asociados a disfunción autonómica tras la activación desregulada de células T.
La correlación está completamente establecida, a pesar de ello todavía no se ha establecido oficialmente la causalidad..
La activación excesiva del sistema inmune innato puede inducir inflamación crónica y desregulación inmunitaria.
Por tanto, en individuos con predisposición genética, la vacunación puede actuar como un desencadenante de enfermedades autoinmunes latentes.
Ejemplo clínico: la activación plaquetaria patológica
Como he mencionado en VITT, los anticuerpos anti-PF4 inducen activación plaquetaria persistente a través del receptor FcγIIa, lo que genera trombosis en sitios inusuales como el seno venoso cerebral o las arterias esplácnicas.
Mimetismo molecular y la posibilidad de autoinmunidad
Algunos estudios han encontrado que la proteína Spike podría compartir epítopos con proteínas del huésped, un fenómeno conocido como mimetismo molecular. Esto podría inducir una respuesta inmune cruzada, generando anticuerpos que reaccionan no solo con el virus sino también con proteínas endógenas, como el PF4. En casos raros, estos anticuerpos pueden persistir y, en el caso de mujeres embarazadas, cruzar la placenta.
De la Madre al Neonato: La Transferencia de Anticuerpos y sus Consecuencias
El embarazo es un estado inmunológico único en el que los anticuerpos IgG maternos atraviesan la placenta para conferir inmunidad pasiva al feto. Este mecanismo, beneficioso en la mayoría de los casos, puede tornarse perjudicial cuando los anticuerpos transferidos tienen potencial patogénico.
1. Mecanismo de la trombosis neonatal mediada por anticuerpos maternos
Los anticuerpos anti-PF4 producidos por la madre cruzan la barrera placentaria.
En el neonato, estos anticuerpos activan las plaquetas, desencadenando la liberación de más PF4.
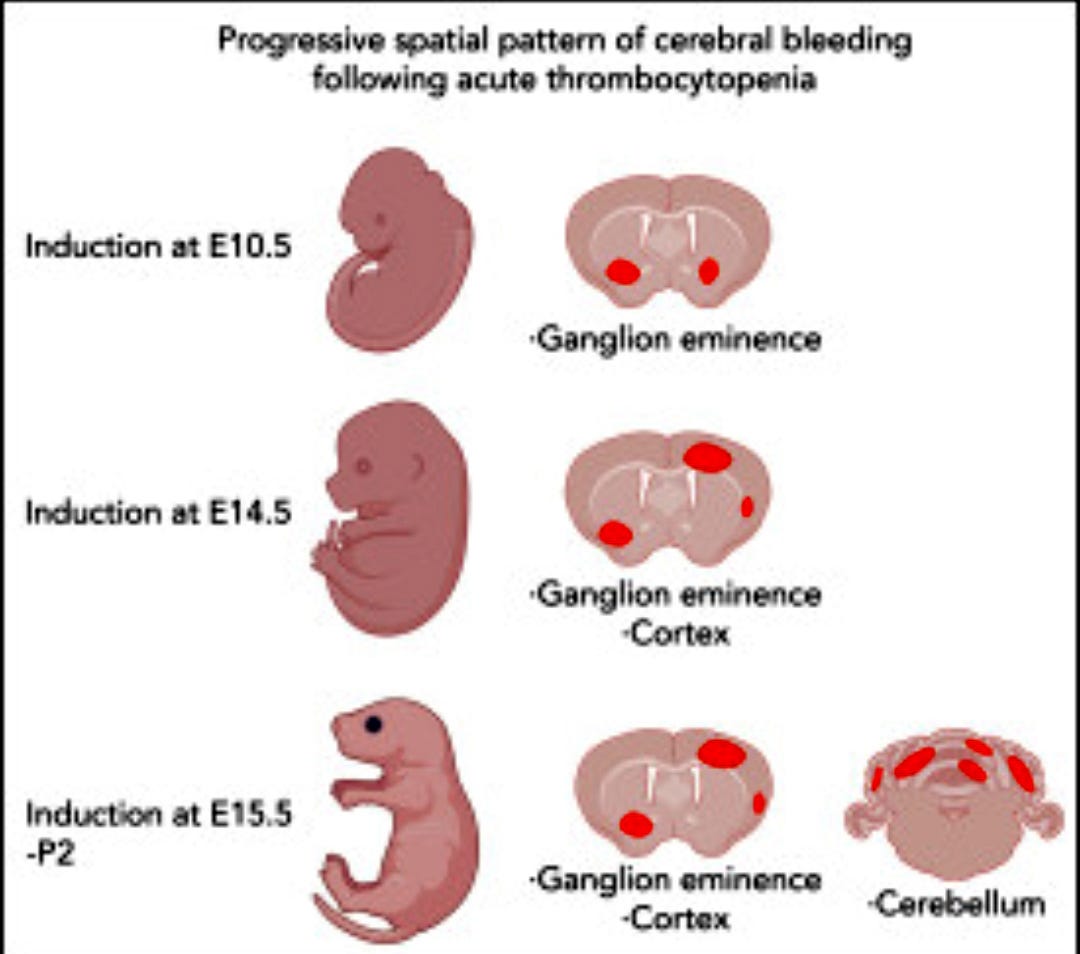
Se forma un ciclo de retroalimentación en el que la activación plaquetaria genera trombos en los vasos cerebrales.
La trombosis del seno venoso cerebral es una de las consecuencias más graves, junto con la trombocitopenia y la hiperfibrinólisis.
2. Factores de riesgo y predisposición
No todas las madres vacunadas desarrollan estos anticuerpos, lo que sugiere que existen factores predisponentes:
Genética individual: Algunas personas tienen una predisposición a generar respuestas inmunes cruzadas.
Estado inflamatorio preexistente: La presencia de infecciones previas o enfermedades autoinmunes podría favorecer la generación de anticuerpos anti-PF4.
Tipo de vacuna recibida: Aunque la mayoría de los casos de VITT se han relacionado con vacunas basadas en adenovirus, se han reportado también eventos con las de ARNm.
Diagnóstico Clínico
Dado el riesgo potencial para neonatos, es fundamental que los médicos adopten estrategias para la detección temprana de esta condición.
1. Identificación de factores de riesgo materno
Antecedentes de vacunación reciente, especialmente con vacunas basadas en adenovirus.
Historia previa de trombosis o desórdenes autoinmunes.
Presencia de síntomas como trombocitopenia inexplicada durante el embarazo.
2. Pruebas diagnósticas en neonatos
Detección de anticuerpos anti-PF4: Se puede realizar mediante ELISA para confirmar su presencia; Fundamental en la sospecha de VITT o trombocitopenia neonatal inducida por anticuerpos maternos.
Estudios de imagen: La resonancia magnética puede revelar trombosis del seno venoso cerebral.
Hemograma: La trombocitopenia neonatal podría ser un signo temprano de activación plaquetaria.
Pruebas de activación plaquetaria (SRA o HIPA): Útiles para confirmar la activación plaquetaria mediada por inmunocomplejos.
Detección de autoanticuerpos contra receptores adrenérgicos y muscarínicos: Puede ser útil en pacientes con disautonomía post vacunación.
El especialista debe en primer lugar hacer:
1. Detección y seguimiento: identificar signos y síntomas iniciales de trastornos de la coagulación en pacientes que acudan a consulta primaria.
2. Educación del paciente: Proporcionan información básica sobre la importancia de la coagulación y los factores que pueden afectarla, incluyendo el papel del PF4.
3. Derivación oportuna: Remitir a los pacientes a especialistas como hematólogos cuando se sospeche de trastornos complejos relacionados con el PF4 o la coagulación.
4. Seguimiento post-hospitalario: Realizar el seguimiento de pacientes que han sido tratados por especialistas por problemas relacionados con la coagulación.
Biomarcadores de Activación del Sistema Inmune
El estudio del perfil inmunológico en pacientes afectados puede proporcionar pistas diagnósticas tempranas:
Niveles elevados de D-dímero: Indican activación de la cascada de coagulación y deben ser considerados en el diagnóstico diferencial de trombosis post vacunación.
Elevación de interleucinas proinflamatorias (IL-6, TNF-α): Sugiere activación inmune sistémica.
PCR ultrasensible y ferritina: Indicadores indirectos de inflamación sistémica persistente
Monitoreo neonatal riguroso: Es esencial vigilar signos de trombosis para intervenir tempranamente.
Las agencias regulatorias y la industria farmacéutica han sostenido que los eventos adversos graves son extremadamente infrecuentes. Sin embargo, la medicina nos enseña que incluso las rarezas estadísticas merecen atención, no solo por su impacto clínico, sino por la confianza que la sociedad deposita en la comunidad médica.
La transparencia en la comunicación de efectos adversos es clave para mantener la confianza en la ciencia.
Se requieren estudios más amplios sobre la autoinmunidad post vacunación para mejorar la selección de pacientes de alto riesgo.
Un enfoque de medicina personalizada, que identifique predisposiciones inmunológicas, puede optimizar la seguridad de los pacientes con condiciones especiales que en los planes de vacunación no se están teniendo en cuenta, cuando se envía la ciudadanía a vacunódromos y se les dice mediante propaganda continua que son seguras y efectivas. La medicina igual para todos que propone Organizaciones como la OMS en detrimento de la medicina personalizada, comporta riesgos éticos que los pacientes no tienen por qué soportar. Solo con una actitud crítica, abierta y rigurosa podremos ofrecer a nuestros pacientes el nivel de cuidado que realmente merecen.
La verdadera ética médica radica en aceptar que no existen certezas absolutas, y que cada descubrimiento es un peldaño más en la construcción de un conocimiento que debe ser, por encima de todo, transparente y basado en la evidencia.
Para solicitar consulta con la Dra. Natalia Prego en (Barcelona; Madrid; Vilagarcía; Pontevdera) o Telemática, escribir al WhatAspp personal: +34 692948272
REFERENCIAS
Häusler Silke, Schönborn L, Gradl J, Cadamuro J, Steinbrücker K, Broto M, Palicio M, Budde K, Wesche J, Greinacher A, Thiele T. Maternal Anti-PF4 Antibodies as Cause of Neonatal Stroke. N Engl J Med. 2025 Feb 13;392(7):719-721. doi: 10.1056/NEJMc2413301. PMID: 39938100
https://www.nejm.org/doi/full/10.1056/NEJMc2413301
Ignacio Cruz-Gonzáleza , María Sánchez-Ledesmaa , Pedro L. Sánchezb e Ik-Kyung JangGreinacher A, Thiele T, Warkentin TE, Weisser K, Kyrle PA, Eichinger S. Trombocitopenia trombótica después de la vacunación con ChAdOx1 nCov-19. https://www.elsevier.es/index.php?p=revista&pRevista=pdf-simple&pii=13111239&r=358
Ignacio Cruz-Gonzáleza , María Sánchez-Ledesmaa , Pedro L. Sánchezb e Ik-Kyung JangGreinacher A, Thiele T, Warkentin TE, Weisser K, Kyrle PA, Eichinger S. Trombocitopenia trombótica después de la vacunación con ChAdOx1 nCov-19.
. N Engl J Med 2021;384:2092-2101. https://www.nejm.org/doi/10.1056/NEJMoa2104840
Antígeno CD184 (CXCR4) https://www.beckman.es/reagents/coulter-flow-cytometry/antibodies-and-kits/single-color-antibodies/cd184
Warkentin TE, Baskin-Miller J, Raybould AL, et al. Adenovirus-associated thrombocytopenia, thrombosis, and VITT-like antibodies. N Engl J Med 2023;389:574-577. https://www.nejm.org/doi/10.1056/NEJMc2307721
Greinacher A, Langer F, Schönborn L, et al. Platelet-activating anti-PF4 antibodies mimic VITT antibodies in an unvaccinated patient with monoclonal gammopathy. Haematologica 2022;107:1219-1221.
https://haematologica.org/article/view/haematol.2021.280366
Rossor T, Arichi T, Bhate S, Hart AR, Raman Singh R. Anticoagulation in the management of neonatal cerebral sinovenous thrombosis: a systematic review and meta-analysis. Dev Med Child Neurol 2018;60:884-891.
https://onlinelibrary.wiley.com/doi/10.1111/dmcn.13760
Schönborn L, Esteban O, Wesche J, et al. Anti-PF4 immunothrombosis without proximate heparin or adenovirus vector vaccine exposure. Blood 2023;142:2305-2314.
Estamos trabajando para crear la Fundación Médicos por la Verdad
Si puede apoye:



Buenos día, Doctora Natalia. En efecto: también en mi ciudad, Mendoza, Argentina, es muy LLAMATIVO que muchas madres primerizas hayan tenido abortos espontáneos luego de la PSEUDO VACUNACIÓN FOZADA con este experimento aplicado en cobayas no siempre voluntarias.
No tiene perdón de Dios esta ABYECTA VIOLACIÓN del derecho a la vida que LOS YA SABEMOS QUIÉNES vienen llevando a cabo desde el nefasto QUINQUENIO 2020/ 2024. Gracias por su fundamentación irrefutable acerca de este experimento cuyo preámbulo fue el TERRORISMO SANITARIO de 2020. "Pensaron ADORMECER al REBAÑO, pero EMPEZAMOS A DESPERTAR LAS OVEJAS..."